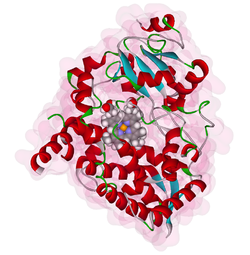
Cytochrom P450 3A4
| Cytochrom P450 3A4 | ||
|---|---|---|
| Strukturmodell von Cytochrom P450 3A4 mit zentraler Hämgruppe nach PDB 1W0E | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 503 AS; 57,3 kDa | |
| Kofaktor | Häm | |
| Bezeichner | ||
| Gen-Name | CYP3A4 | |
| Externe IDs | OMIM: 124010 UniProt: P05184 | |
| Enzymklassifikationen | ||
| EC, Kategorie | 1.14.13.32 Monooxygenase | |
| Reaktionsart | Oxidation | |
| Substrat | Albendazol + NADPH/H+ + O2 | |
| Produkte | Albendazol-S-oxid + NADP+ + H2O | |
| EC, Kategorie | 1.14.13.67 Monooxygenase | |
| Reaktionsart | Hydroxylierung | |
| Substrat | Chinin + NADPH/H+ + O2 | |
| Produkte | 3-Hydroxychinin + NADP+ + H2O | |
| EC, Kategorie | 1.14.13.97 Monooxygenase | |
| Reaktionsart | Hydroxylierung | |
| Substrat | Lithocholat + NADPH/H+ + O2 | |
| Produkte | Hyocholat + NADP+ + H2O | |
| Vorkommen | ||
| Übergeordnetes Taxon | Wirbeltiere | |
Cytochrom P450 3A4 (abgekürzt: CYP 3A4), ist ein Isoenzym der Cytochrom P450-Superfamilie. Es ist im menschlichen Körper einer der zentralen Bestandteile der Verstoffwechselung (Biotransformation) insbesondere körperfremder Stoffe (Xenobiotika). Cytochrom P450 3A4 kommt mengenmäßig am meisten in der Leber vor. Es hat die meisten Substrate aller Cytochrome. Da auch viele Arzneistoffe über Cytochrom P450 3A4 abgebaut werden, ist es das Zentrum vieler Arzneimittelinteraktionen.
Genetik
Bei Menschen ist Cytochrom P450 3A4 auf dem CYP3A4-Gen codiert.[1] Diese Gen liegt neben vielen anderen Cytochromgenen auf Chromosom 7q21.1.[2]
Funktion
Cytochrom P450-Enzyme sind fast ausschließlich Monooxygenasen, die eine Hydroxylierung katalysieren. Neben der Synthese von Steroiden und Steroidhormonen ist diese Reaktion in der Biotransformation wichtig um hydrophobe Stoffe wasserlöslich und damit ausscheidbar zu machen. Zusätzlich spielt es eine große Rolle bei Medikamenten, die als Prodrug verabreicht werden. Hierbei wird durch die Enzymkatalyse die aktive Form gebildet. Bei einer Inhibition von CYP 3A4 wird demnach das aktive Medikament nicht, oder nur vermindert gebildet.
Dadurch, dass viele Medikamente über dasselbe Isoenzym abgebaut werden, treten dort besonders viele Arzneimittelinteraktionen auf. Einige Stoffe induzieren das Enzym, andere hemmen es. Durch eine Enzymhemmung können die von ihm abgebauten Stoffe kumulieren, das kann so weit gehen, dass dadurch die toxische Schwelle überschritten wird. Bei einer Enzyminduktion kann ein Substrat soweit abgebaut werden, dass der Blutplasma-Wirkspiegel nicht mehr erreicht wird.
Substrate
Induktoren
- Hyperforin im Johanniskraut[4]
- Ingwer
- Knoblauch
- Lakritze
- Rifampicin (Antibiotikum)
- Antikonvulsiva & Stimmungsaufheller
- Phenobarbital
- Modafinil
Hemmer
- Bergamottin in Grapefruitsaft[5]
- Baldrian
- Gelbwurzel
- Ginseng
- viele Antibiotika
- Antimykotika (Fluconazol, Ketoconazol, Itraconazol)
- Proteasehemmer aus der HIV-Therapie (Ritonavir, Indinavir, Nelfinavir)
- Aprepitant (Antiemetikum)
- Verapamil (Calciumkanal-Blocker)
- Nefazodon (Antidepressivum)
Beispiele für Interaktionen
Eine Organtransplantation verlangt nach Immunsuppression um eine Transplantatabstoßung zu verhindern. Die meisten Immunsupressiva werden durch CYP3A4 verstoffwechselt, was dazu führt, dass die gleichzeitige Einnahme von Johanniskraut, z.B. im Rahmen einer leichten depressiven Episode zu einer Plasmaspiegelabnahme des Immunsupressivums führt und ggf. bis zu einer Abstoßungsreaktion mit Organversagen führen kann.
Weblinks
- Die Cytochrom-P450-Superfamilie auf KEGG
- Indiana University - School of Medicine: Liste mit verstoffwechselten Arzneimitteln, Enzyminduktoren und Enzymhemmern für die einzelnen Isoenzyme
- Arzneimittelinteraktionen (engl.)
Einzelnachweise
- ↑ Hashimoto H, Toide K, Kitamura R, Fujita M, Tagawa S, Itoh S, Kamataki T: Gene structure of CYP3A4, an adult-specific form of cytochrome P450 in human livers, and its transcriptional control. In: Eur. J. Biochem.. 218, Nr. 2, Dezember 1993, S. 585–95. doi:10.1111/j.1432-1033.1993.tb18412.x. PMID 8269949.
- ↑ Inoue K, Inazawa J, Nakagawa H, Shimada T, Yamazaki H, Guengerich FP, Abe T: Assignment of the human cytochrome P-450 nifedipine oxidase gene (CYP3A4) to chromosome 7 at band q22.1 by fluorescence in situ hybridization. In: Jpn. J. Hum. Genet.. 37, Nr. 2, Juni 1992, S. 133–8. doi:10.1007/BF01899734. PMID 1391968.
- ↑ Druglib.com
- ↑ Thomas Effert: Molekulare Pharmakologie und Toxikologie: Biologische Grundlagen von Arzneimitteln und Giften, S. 24. Springer, Berlin 2006, ISBN 9783540212232.
- ↑ Pharmazeutische Zeitung online 35/2008: Grapefruit - Neuer Interaktionsmechanismus entdeckt. Abgerufen am 10. Januar 2011.
- ↑ Park JY, Kim KA, Kim SL: Chloramphenicol is a potent inhibitor of cytochrome P450 isoforms CYP2C19 and CYP3A4 in human liver microsomes. In: Antimicrob. Agents Chemother.. 47, Nr. 11, November 2003, S. 3464–9. doi:10.1128/AAC.47.11.3464-3469.2003. PMID 14576103. Volltext bei PMC: 253795.
| Bitte den Hinweis zu Gesundheitsthemen beachten! |