14. Besondere Verbrennungserscheinungen - Feuerlöschen
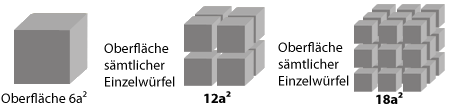
Stahlwolle kann sehr leicht mit einem Streichholz entzündet werden. Bläst man Aluminiumpulver in eine Flamme, verbrennt es mit einer Stichflamme. Offensichtlich reagieren fein verteilte, pulverisierte Stoffe schneller als Stoffe, die in kompakten Einzelstücken vorliegen. Pulverisierte Stoffe besitzen eine viel größere Oberfläche, daher verbinden sich bei der Verbrennung die Sauerstoffmoleküle viel schneller mit den feinen Teilchen des Feststoffes.
In Versuch 2 wird Holzstaub von der Kerzenflamme entzündet. Der Verbrennungsvorgang läuft dabei so schnell ab, dass es zur Explosion kommt. Solche gefählichen Staubexplosionen treten vermehrt in Kohlebergwerken, Mühlen oder holzverarbeitenden Betrieben auf (Mehlstaubexplosion in der Rolandmühle im Februar 1979 in Bremen). Schon durch den elektrischen Funken beim Umlegen eines Lichtschalters kann trockener, brennbarer Staub explodieren, genauso verhält es sich bei Kunstoffen durch Reibungselektrizität. Gemische aus brennbaren Gasen und Luft sind besonders explosiv, da Gase die größte Oberfläche besitzen Gase (Versuch 2, Kapitel 13).
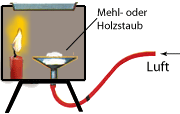
Versuchsaufbau zur Demostration einer Staubexplosion. Mit dieser Versuchsanordnung kann eine Staubexplosion vorgeführt werden.
In einem Gebäude mit defekten, undichten Gasleitungen können Gasgemische entstehen, die bei der Zündung durch einen Lichtschalter, einen Kurzschluss oder durch ein Streichholz so heftig explodieren, dass das Gebäude unter der Wucht der Explosion einstürzt. »Schlagwetterexplosionen« in Bergwerken werden durch unerwartet austretendes Grubengas ausgelöst, dabei kann ein 5,5%-13,5%iges Gemisch aus Grubengas und Luft schon durch Funkenbildungen gezündet werden, die beim Schlag eines Hammers auf Stein entstehen.
Eine kontrollierte Explosion läuft im Zylinder eines Verbrennungsmotor ab. Hier wird ein Gemisch von Treibstoff und Luft durch die Zündkerzen gezündet. Die dabei entstehende Energie wird über mehrere Stationen dann auf die Räder übertragen.
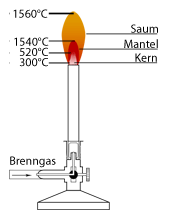
Die Flamme eines Bunsenbrenners ist brennendes Gas, meist handelt es sich um Leuchtgas, Erdgas oder Propangas. Über eine Zuleitung im Standfuß wird das Gas dem Brenner zugeführt und steigt mit hoher Geschwindigkeit durch eine Düse in den Mischkamin, wo es sich mit Luft vermischt. Die Menge der Luft, die sich mit dem Gas vermischen soll, kann durch eine Stellschraube eingestellt werden. Dies ist besonders wichtig, da die Temperatur der Flamme von der Gasart und dem Anteil der zugeführten Luft abhängt.
Die Flamme einer Kerze ist ebenfalls brennendes Gas. Das flüssige Kerzenwachs steigt im Docht nach oben. Mit zunehmender Hitze geht es in den Dampfzustand über und verbrennt.
Die langsame Verbrennung
An der Luft verlieren etliche Metalle, beispielsweise Kupfer, Eisen oder Zink schnell ihren typischen Metallglanz und auf der Oberfläche bildet sich langsam eine Schicht aus Metalloxid. Dieser Vorgang wird als langsame Verbrennung bezeichnet, denn sie läuft ohne Feuererscheinung und unterhalb der Entzündungstemperatur ab. Ein bekanntes Beispiel ist der Eisenrost, der durch eine langsame Verbrennung entsteht.
Bei der Atmung werden Kohlenstoffverbindungen verbrannt, auch sie ist eine langsam ablaufende Verbrennung, bei der die gewonnene Energie dem Organismus zur Aufrechterhaltung der Lebensfunktionen dient. Bei der Atmung entsteht Kohlenstoffdioxid, diese Tatsache kann man mit Versuch Versuch 4 nachweisen, in dem Kalkwasser eine Trübung erfährt.
Feuerlöschen
Ein Brand kann gelöscht werden, wenn es gelingt, 1.) die Entzündungstemperatur des brennenden Stoffes zu unterschreiten, und 2.) den Zutritt von Sauerstoff stark oder ganz herabzusetzen.
Beim Löschen mit Wasser werden zwar beide Bedingungen erfüllt, jedoch können brennende Flüssigkeiten nicht mit Wasser gelöscht werden. In diese Fall muß die Sauerstoffzufuhr durch Sand oder feuerfeste Decken unterbrochen werden. Ein kleinerer Brand kann mit mit Kohlenstoffdioxid oder Stickstoff aus Stahlflaschen gut gelöscht werden.
Beim Schaumlöschen (Versuch 5) sprüht man einen kohlenstoffdioxidhaltigen Schaum auf den Brandherd. Beim Trockenlöschen verstreut man ein Pulver, das unter Wärmeeinwirkung Kohlenstoffdioxid abgibt, auf den Brandherd. Beide Löschmethoden finden in den handelsüblichen Feuerlöschgeräten Anwendung.
