15. Die Zusammensetzung der Luft
Nachweis des Sauerstoffanteils
Luft ist ein Gasgemisch, das zum überwiegenden Teil aus den Elementen Stickstoff und Sauerstoff besteht. Versuch 1 zeigt, dass etwa $\tfrac {1} {5}$ des Volumens der Luft aus Sauerstoff besteht. Im Kolbenproberversuch hat sich das Kupfer in der Hitze mit dem Sauerstoff der Luft zu schwarzem Kupferoxid verbunden:
$ \mathrm { 2Cu+O_{2} \longrightarrow 2CuO } $
Kupfer + Sauerstoff → Kupferoxid
Der Hauptbestandteil der Luft ist Stickstoff. Neben Sauerstoff enthält sie noch das Treibhausgas Kohlenstoffdioxid und die fünf Edelgase. Eine genaue Analyse der Luft ist in der Tabelle unten zu sehen.
| Anteil | Vol.% | Siedep. °C | Schm. °C | Litermasse g / l |
| Stickstoff | 78,09 | - 196 | - 210 | 1,25 |
| Sauerstoff | 20,95 | - 183 | - 218 | 1,43 |
| Kohlenstoffdioxid | 0,03 | - 78,5 | bei 5,3 bar -57 | 1,98 |
| Helium | 0,00046 | - 269 | - | 0,178 |
| Neon | 0,00161 | - 246 | - 249 | 0,899 |
| Argon | 0,9325 | - 186 | - 189 | 1,788 |
| Krypton | 0,000108 | - 153 | - 157 | 3,736 |
| Xenon | 0,000008 | - 107 | - 112 | 5,891 |
Luftverflüssigung
Man kann durch Verbrennungsreaktionen den Sauerstoff der Luft auf chemischem Wege von den übrigen Luftbestandteilen trennen. Die Zerlegung der Luft in ihre Bestandteile geschieht auf physikalischem Weg.

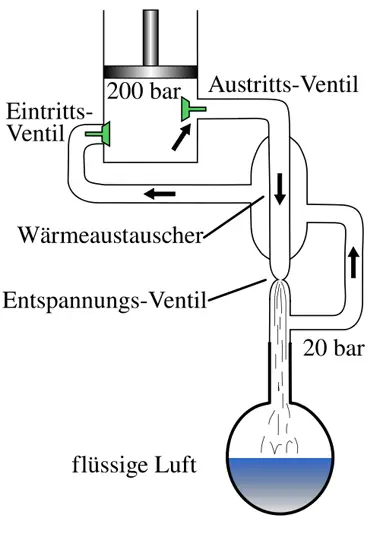
Dazu wird die Luft zuerst verflüssigt. Sie wird zunächst von Wasserdampf, Staub und Kohlenstoffdioxid befreit. Ein Kompressor verdichtet die Luft dann auf einen Druck von 200 bar. Anschließend wird die Luft über ein Expansionsventil oder einer Turbine entspannt, wobei ihre Temperatur im ersten Schritt um ca. 45 K auf ca. −25 °C sinkt. Diese abgekühlte Luft wird über einen Gegenstrom-Wärmeübertrager in den Kompressor zurückgeleitet und dient somit zur Kühlung weiterer komprimierter Luft vor deren Entspannung. Durch diesen Prozess wird die Luft allmählich so tief gekühlt, dass bei 20 bar die Verflüssigung eintritt.

Dieser heute als Linde-Verfahren bezeichnete Prozess geht auf den deutschen Ingenieur Carl von Linde (1842 - 1934) zu rück. Flüssige Luft kann mittels Fraktionieren in ihre Bestandteile zerlegt werden: Man nutzt die unterschiedlichen Siedepunkte der einzelnen Luftbestandteile aus. Allerdings liegen die Siedepunkte von Sauerstoff und Stickstoff sehr dicht zusammen. Das Verfahren nennt man fraktionierte Destillation flüssiger Luft und in der Technik verwendet man diesen Prozess für die Gewinnung von Stickstoff und Sauerstoff, aber auch von Edelgasen.
Die Edelgase
Die Edelgase sind die Elemente Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe) und Radon (Rn). Edelgase gehen unter normalen Umständen keine chemischen Verbindungen ein, alle sind außerordentlich reaktionsträge und auf dieses Verhalten geht auch die Bezeichnung Edelgas zurück. Vor 1962 galten alle Edelgase als inert, als chemische Stoffe, die keine Verbindungen eingehen. Zwischenzeitlich sind viele weitere Edelgasverbindungen bekannt geworden. Wegen ihres »edlen« (trägen) Verhaltens gehen sie auch untereinander keine Verbindungen ein und treten immer einatomig auf. Da Edelgase in vielen wesentlichen Eigenschaften übereinstimmen, gruppiert man sie in einer Elementfamilie.
Edelgase finden seit langem in so unterschiedlichen Bereichen wie der Beleuchtungstechnik (»Neonröhren«) und dem Tauchsport Anwendung. Helium beispielsweise ist nicht brennbar und dient als Traggas für Ballone und Luftschiffe. Wegen seiner Nichtbrennbarkeit bewährt sich Helium als Traggas für Luftschiffe und Ballone; allerdings steht es nur in sehr begrenztem Umfang zur Verfügung. Benannt wurde Helium nach der Sonne (griech.: „helios“), da es bei der totalen Sonnenfinsternis von 1868 durch P. Janssen im Spektrum der Sonnenprotuberanzen entdeckt wurde. Argon hat als Schutzgas beim Schweißen große Bedeutung.
Luftzerlegung und Umweltschutz bei der Linde AG
Zur Schonung von natürlichen Ressourcen und Vermeidung indirekter Treibhausgasemissionen arbeitet Linde laufend an der Optimierung seiner Luftzerlegungsanlagen. Geachtet wird dabei vor allem auf die Senkung des Energiebedarfs sowie die Verbesserung der Ressourceneffizienz unter Beibehaltung der jeweiligen Produktionskapazität. Dies geschieht zum Beispiel weltweit durch die verbesserte Anlagensteuerung, die Nutzung von energiesparenden Turbokompressoren oder die Senkung des Energiebedarfs für das Kühlwasser sowie dessen Recycling. Zur Motivierung der Ingenieure werden die energieeffizientesten Luftzerlegungsanlagen ausgezeichnet. Die umwelt- und klimaschutzrelevanten Daten der Luftzerlegungsanlagen werden kontinuierlich gemessen und jährlich veröffentlicht. Weitere Informationen stehen im Internet unter www.linde.com/sustainability und im Linde Corporate Responsibility Report zur Verfügung.