Calciumbromid
| Kristallstruktur | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
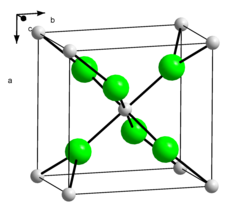
| |||||||||||||||
| __ Ca+ __ Br− | |||||||||||||||
| Allgemeines | |||||||||||||||
| Name | Calciumbromid | ||||||||||||||
| Andere Namen |
Calciumdibromid | ||||||||||||||
| Verhältnisformel | CaBr2 | ||||||||||||||
| CAS-Nummer |
| ||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||
| Eigenschaften | |||||||||||||||
| Molare Masse | 199,88 g·mol−1 | ||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||
| Dichte |
3,353 g·cm−3[2] | ||||||||||||||
| Schmelzpunkt |
730 °C [2] | ||||||||||||||
| Siedepunkt |
806-812 °C [2] | ||||||||||||||
| Löslichkeit |
gut löslich in Wasser: 1420 g·l−1 (20 °C)[2] | ||||||||||||||
| Sicherheitshinweise | |||||||||||||||
| |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||
Calciumbromid ist eine chemische Verbindung des Calciums und zählt zu den Bromiden. Es ist ein farbloser, an der Luft sich langsam gelb färbender Feststoff.
Gewinnung und Darstellung
Calciumbromid lässt sich durch Reaktion von Calciumcarbonat, Calciumoxid oder Calciumhydroxid mit Bromwasserstoff gewinnen.[4]
Eine Alternative ist die Umsetzung der Calciumsalze mit Brom und einem Reduktionsmittel wie Ameisensäure oder Formaldehyd.[4]
Eigenschaften
Calciumbromid kristallisiert wie Calciumchlorid und Strontiumchlorid in der Calciumchloridstruktur, die der Rutilstruktur ähnlich ist. Im gasförmigen Zustand bidet es lineare Moleküle.[5]
An der Luft färbt sich die Verbindung langsam gelb, da sich elementares Brom bildet. Calciumbromid ist in Wasser und Methanol gut, in Ether und Chloroform nur in geringem Maß löslich.[6]
Verwendung
Auf Grund seiner Dichte wird Calciumbromid vorwiegend in Bohrspülmitteln bei der Förderung von Erdöl und Erdgas eingesetzt. Daneben wird es zur Herstellung von Photoplatten, als Arzneimittel, in Holzschutz-, sowie in Flammschutzmitteln eingesetzt.[4]
Einzelnachweise
- ↑ 1,0 1,1 1,2 Datenblatt Calciumbromid bei Sigma-Aldrich, abgerufen am 15. März 2011.
- ↑ 2,0 2,1 2,2 2,3 2,4 Datenblatt Calciumbromid bei AlfaAesar, abgerufen am 9. Juni 2009 (JavaScript erforderlich).
- ↑ Seit 1. Dezember 2012 ist für Stoffe ausschließlich die GHS-Gefahrstoffkennzeichnung zulässig. Bis zum 1. Juni 2015 dürfen noch die R-Sätze dieses Stoffes für die Einstufung von Zubereitungen herangezogen werden, anschließend ist die EU-Gefahrstoffkennzeichnung von rein historischem Interesse.
- ↑ 4,0 4,1 4,2 M.J. Dagani, H.J. Barda, T.J. Benja, D.C. Sanders: Bromine Compounds. In: Ullmanns Enzyklopädie der Technischen Chemie. Wiley-VCH, Weinheim 2005, doi:10.1002/14356007.a04_405, S. 22.
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1241.
- ↑ Calciumbromid. In: Römpp Chemie-Lexikon, Thieme Verlag, Stand März 2002.