Furan
| Strukturformel | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | |||||||||||||||||||||
| Name | Furan | ||||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||||
| Summenformel | C4H4O | ||||||||||||||||||||
| CAS-Nummer | 110-00-9 | ||||||||||||||||||||
| PubChem | 8029 | ||||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit von chloroformartigem Geruch[1] | ||||||||||||||||||||
| Eigenschaften | |||||||||||||||||||||
| Molare Masse | 68,08 g·mol−1 | ||||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||||
| Dichte |
0,94 g·cm−3 [2] | ||||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||||
| Siedepunkt |
32 °C [2] | ||||||||||||||||||||
| Dampfdruck | |||||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (10 g·l−1 bei 20 °C) [2] | ||||||||||||||||||||
| Brechungsindex |
1,421 (20 °C)[3] | ||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||
| |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||||
Furan (Furfuran) ist eine in Wasser schlecht lösliche organische Flüssigkeit aus der Gruppe der Sauerstoffheterocyclen bzw. Enolether.
Geschichte
Der Name Furan leitet sich vom lateinischen Wort furfur für Kleie ab.[6] Als erstes Furanderivat stellte der Chemiker Carl Wilhelm Scheele 1780 Furan-2-carbonsäure (Brenzschleimsäure) her. Johann Wolfgang Döbereiner berichtete 1831 von einem weiteren wichtigen Derivat, dem Furfural, neun Jahre später konnte es der schottische Chemiker John Stenhouse charakterisieren. Furan stellte 1870 der Chemiker Heinrich Limpricht her. Er nannte es fälschlicherweise Tetraphenol.[7][8]
Die Weltgesundheitsorganisation (WHO) hat Furan als möglicherweise Krebs erregend für den Menschen eingestuft. Die genaue Wirkung im menschlichen Körper muss allerdings noch geklärt werden.
Gewinnung und Darstellung
Furan wird technisch aus Furfural (Furan-2-carbaldehyd) hergestellt. Dieses kann durch Destillation von Kleie mit Schwefelsäure gewonnen werden. Zur Decarbonylierung (Abspaltung von Kohlenstoffmonoxid) des Furfurals wird es zusammen mit Zinkoxid und Chrom(III)-oxid auf 400 °C erhitzt. In einem alternativen Syntheseweg wird das Furfural zunächst mit Sauerstoff zur Furan-2-carbonsäure oxidiert und anschließend durch eine Decarboxylierung zu Furan umgesetzt. Eine weitere Möglichkeit zur Synthese von Furan und seinen Derivate bietet die Umsetzung von 1,4-Dicarbonylverbindungen (für Furan wird Butandial benötigt) mit trockenem HCl-Gas oder mit Phosphor(V)-oxid [9]
Eigenschaften
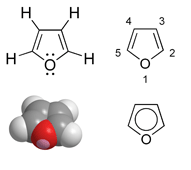
Furan ist ein Aromat, ein Fünfring mit Sauerstoff als Heteroatom. Es besitzt sechs π-Elektronen, vier in den Doppelbindungen und zwei in einem freien Elektronenpaar des sp2-hybridisierten Sauerstoffs. Somit gehört es zu den Heteroaromaten und zu den Heterocyclen. Der aromatische Charakter ist jedoch schwächer als bei Pyrrol und Thiophen ausgeprägt.
Furan hat einen niedrigen Siedepunkt (32 °C) und schon bei Raumtemperatur einen hohen Dampfdruck. Es ist brennbar und – wegen des hohen Dampfdrucks – hochentzündlich.
Verwendung
Eine wichtige Reaktion des Furans ist die Hydrierung zum cyclischen Ether Tetrahydrofuran, der oft als Lösungsmittel verwendet wird.
Furanharze werden beim Gießen, mit Sand vermischt, als Formwerkstoff in den Formkästen eingesetzt.
Furan ist unter anderem im Kaffee enthalten und dient dort als Geschmacksträger, was in einer Dokumentation der Reihe ZDFzoom, die sich auf wissenschaftliche Untersuchungen beruft, als ein mögliches Gesundheitsrisiko eingestuft wurde. Der Furangehalt ist dabei direkt von der angewandten Brühmethode abhängig.[10]
Derivate
Furanderivate kommen in Aromen und Riechstoffen vor und wirken in der Natur als Pheromone. Furanfettsäuren werden von verschiedenen Pflanzen aus Fettsäuren synthetisiert und lassen sich in einer Vielzahl von Organismen nachweisen.
Ähnliche Strukturen bilden einige Kohlenhydrate (Zucker), diese werden als Furanosen bezeichnet, enthalten jedoch keine Doppelbindungen im Ring.
Siehe auch
- Benzofuran, Furan mit einem kondensierten Benzolring.
- Dibenzofuran, die Grundstruktur der Stoffklasse der polychlorierten Dibenzofurane.
- Furanocumarine
- Pyrrol, die Entsprechung des Furans, die Stickstoff enthält statt Sauerstoff.
- Tetrahydrofuran (THF), die vollständig hydrierte Entsprechung des Furans und ein gebräuchliches Lösungsmittel.
- Thiophen, die Schwefel-Entsprechung des Furans.
- 2,5-Dimethylfuran
Einzelnachweise
- ↑ Römpp CD 2006, Georg Thieme Verlag 2006
- ↑ 2,0 2,1 2,2 2,3 2,4 Eintrag zu Furan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 16. Mai 2008 (JavaScript erforderlich)
- ↑ 3,0 3,1 Datenblatt Furan bei Sigma-Aldrich, abgerufen am 2. April 2011.
- ↑ 4,0 4,1 Eintrag aus der CLP-Verordnung zu CAS-Nr. 110-00-9 in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich)
- ↑ Seit 1. Dezember 2012 ist für Stoffe ausschließlich die GHS-Gefahrstoffkennzeichnung zulässig. Bis zum 1. Juni 2015 dürfen noch die R-Sätze dieses Stoffes für die Einstufung von Zubereitungen herangezogen werden, anschließend ist die EU-Gefahrstoffkennzeichnung von rein historischem Interesse.
- ↑ Alexander Senning. Elsevier's Dictionary of Chemoetymology. Elsevier, 2006. ISBN 0-444-52239-5.
- ↑ H. Limpricht: Ueber das Tetraphenol C4H4O. In: Berichte der deutschen chemischen Gesellschaft. 3, Nr. 1, 1870, S. 90–91, doi:10.1002/cber.18700030129.
- ↑ Ernest Harry Rodd: Chemistry of Carbon Compounds: A Modern Comprehensive Treatise. Elsevier, Amsterdam, New York 1971.
- ↑ Eberhard Breitmaier, Günther Jung: Organische Chemie. 4. Auflage, Thieme, Stuttgart 2001, ISBN 3-13-541504-X, S. 644.
- ↑ Mögliches Risiko im Kaffee. ZDF.de, 26. September 2012, abgerufen am 6. Oktober 2012.