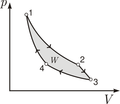
Isotherme Zustandsänderung
- Seiten mit Math-Fehlern
- Seiten mit Math-Renderingfehlern
- Thermodynamischer Prozess
Die isotherme Zustandsänderung ist eine thermodynamische Zustandsänderung, bei der die Temperatur unverändert bleibt. Bei einer Verdichtung eines Gases muss also die Kompressionswärme abgeführt bzw. bei einer Expansion Wärme zugeführt werden. Dies kann durch ein Wärmebad näherungsweise erreicht werden. Nach dem Gesetz von Boyle-Mariotte und der Zustandsgleichung eines idealen Gases bleibt das Produkt aus Druck Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): p und Volumen $ V $ bei konstanter Temperatur T ebenfalls konstant:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): p \cdot V = n \cdot R \cdot T = const. \quad \Leftrightarrow \quad p \sim {1 \over V} .
Daraus folgt auch, dass sich die Drücke umgekehrt proportional zu den entsprechenden Volumina verhalten:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {V_1 \over V_2}={p_2 \over p_1}
Für die verrichtete Arbeit Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta W gilt bei einer isothermen Kompression oder Expansion von Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): n mol eines idealen Gases:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta W = n R T\ln\left({V_1 \over V_2}\right) = n R T \ln\left({p_2 \over p_1}\right) = - p_1 V_1 \ln\left({V_2 \over V_1}\right) ,
wobei Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): R die Universelle Gaskonstante bezeichnet. Nach dem ersten Hauptsatz der Thermodynamik (Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta U = \Delta Q + \Delta W ) folgt mit $ T_{2}=T_{1} $ (und somit Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta T = 0 ), dass die zugeführte bzw. entzogene Wärme direkt der verrichteten Arbeit entspricht (Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta Q = - \Delta W ). Daraus folgt Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): \Delta U=0 , wobei Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): U die innere Energie darstellt.
Siehe auch
Weblinks
adiabatisch | diabatisch · isenthalp · polytrop: isobar | isochor | isotherm | isentrop