Epitop
Ein Epitop (griech. ἐπί epi „bei, auf“ und τόπος topos „Ort“, synonym: antigene Determinante) ist ein Bereich der Oberfläche eines Antigens, an den ein Antikörper oder T-Zell-Rezeptor spezifisch bindet. Antikörper sind normalerweise gegen Proteine bzw. Proteide gerichtet. In seltenen Fällen können auch Antikörper gegen andere chemische Strukturen (z. B. DNA, Saccharide, Schwermetalle, Steroidhormone, Penicillin) gebildet werden. Die dem Epitop gegenüberliegende Fläche auf dem gebundenen Antikörper oder T-Zell-Rezeptor wird als Paratop bezeichnet.
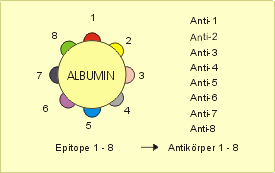
Ein einzelnes Antigen, wie z. B. ein Membranprotein einer Zelle oder eines Bakteriums, trägt verschiedene räumliche Epitope. Gegen jedes dieser Epitope kann ein spezifischer Antikörper oder eine spezifische T-Zelle gebildet werden. Epitope können art- bzw. individualspezifisch sein.
Nach der Phagozytose der Antigene durch Antigen-präsentierende Zellen präsentieren diese die Epitope auf ihrer Zelloberfläche. Anschließend erfolgt die adaptive Immunantwort.
Eigenschaften
Typischerweise besitzen Epitope, welche an MHC-Klasse-I Molekülen gebunden sind, eine Länge von 8–11 Aminosäuren, wohingegen MHC-Klasse-II Epitope längere Peptidketten von circa 15 Aminosäuren aufweisen.
Es wird zwischen kontinuierlichen (synonym Sequenzepitope) und diskontinuierlichen Epitopen (synonym Konformationsepitope) unterschieden. Proteine bestehen aus Aminosäureketten und sind dreidimensional gefaltet. So können Epitope aus verschiedenen, im Raum nah bei einander liegenden Aminosäureresten bestehen, die aber in der Aminosäuresequenz eigentlich weit voneinander entfernt sind. Solche Epitope werden diskontinuierlich genannt, da sie nur im nativen Zustand des Proteins vorhanden sind und erkannt werden können. Bei einer SDS-Gelelektrophorese und anschließendem Western Blot zum Beispiel werden die Aminosäureketten entfaltet (Denaturierung) und die Antikörper binden nicht mehr an diskontinuierliche Epitope, wenn die Epitope sich nicht erneut in die korrekte, native Form falten konnten. Kontinuierliche Epitope bleiben dagegen auch nach einer Denaturierung bestehen, da sie aus einer Sequenz aufeinanderfolgender Aminosäuren bestehen, welche bei der Denaturierung erhalten bleibt.
Die Bindungsspezifität von einem Antikörper an sein Epitop wird als Affinität, die Summe der Bindungsenergien aller an ein Antigen (mit mehreren Epitopen) bindenden Antikörper wird dagegen als Avidität bezeichnet.
Anwendung
In der Gentechnologie finden Epitope tags Anwendung (z. B. His-Tag, Myc-tag, Strep-Tag, V5-Tag oder Flash-tag), um als Fusionsprotein den Nachweis von Proteinen zu ermöglichen, für die kein geeigneter Antikörper zur Verfügung steht. Hierzu wird in den selben Leseraster wie das zu untersuchende Protein das Gen eines Epitops eingebaut, sodass das exprimierte Protein ein N- oder C-terminales Epitope tag erhält. Gegen das angehängte Epitop kann nun ein Antikörper zur Detektion eingesetzt werden. Das gleiche Epitop kann in verschiedenen Versuchen immer wieder an neue Proteine angehängt werden, und somit kann auch immer der gleiche Antikörper verwendet werden, was eine erhebliche Aufwands- und Kosteneinsparung darstellt.
Die Immune Epitope Database ist eine Online-Datenbank für bereits beschriebene Epitope, daneben werden auch Programme zur Vorhersage der Bindungsaffinität von Epitopen an MHC-Moleküle angeboten (Reverse Immunologie). Die systematische Untersuchung der Epitope in einem Antigen wird als Epitopkartierung bezeichnet.
Literatur
- Janeway et al.: Immunobiology. 6. Auflage ISBN 0-8153-4101-6. Die 5. englische Ausgabe ist online auf den Seiten des NCBI-Bookshelf verfügbar, (online).