Niob(V)-chlorid
| Strukturformel | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||
| Allgemeines | |||||||||||||||||
| Name | Niob(V)-chlorid | ||||||||||||||||
| Andere Namen |
Niobpentachlorid | ||||||||||||||||
| Summenformel | NbCl5 | ||||||||||||||||
| CAS-Nummer | 10026-12-7 | ||||||||||||||||
| Kurzbeschreibung |
gelber Feststoff mit stechendem Geruch[1] | ||||||||||||||||
| Eigenschaften | |||||||||||||||||
| Molare Masse | 270,17 g·mol−1 | ||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||
| Dichte |
2,75 g·cm−3[1] | ||||||||||||||||
| Schmelzpunkt | |||||||||||||||||
| Siedepunkt |
248,2 °C[1] | ||||||||||||||||
| Löslichkeit |
heftige Zersetzung in Wasser[1] | ||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||
| |||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||
Niob(V)-chlorid ist eine salzartige chemische Verbindung bestehend aus den Elementen Niob und Chlor.
Eigenschaften

Es handelt sich um einen gelben Feststoff mit stechendem Geruch, der sich heftig in Wasser zersetzt.
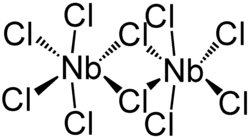
Niob(V)-chlorid bildet eine dimere Struktur aus, bei welcher jedes Niobatom sechsfach durch Chlorido-Liganden koordiniert ist. Zwei Chloratome fungieren als Brückenliganden. Es wird eine verzerrt-oktaedrische Struktur ausgebildet, bei der die pseudo-axialen Chloridoliganden in einem Winkel von 83,7 ° zur pseudo-equatorialen Ebene angeordnet sind.[3]
Verwendung
Niob(V)-chlorid wird in der organischen Chemie als Lewis-Säure verwendet. So findet es beispielsweise in der Aktivierung von Alkenen in der Carbonyl-En-Reaktion Anwendung.[4]
Einzelnachweise
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 Eintrag zu CAS-Nr. 33797-51-2 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10.05.2008 (JavaScript erforderlich)
- ↑ Seit 1. Dezember 2012 ist für Stoffe ausschließlich die GHS-Gefahrstoffkennzeichnung zulässig. Bis zum 1. Juni 2015 dürfen noch die R-Sätze dieses Stoffes für die Einstufung von Zubereitungen herangezogen werden, anschließend ist die EU-Gefahrstoffkennzeichnung von rein historischem Interesse.
- ↑ F. A. Cotton, P. A. Kibala, M. Matusz, R. B. W. Sandor in: Structure of the Second Polymorph of Niobium Pentachlorid 1997, Acta Cryst. C47, 2435–2437.
- ↑ C. K. Z. Andrade, O. E. Vercillo, J. P. Rodrigues, D. P. Silveira in: J. Braz. Chem. Soc. 2004, 15, 6, 813–817.
