Mesomerer Effekt
Nach einer Substitutionsreaktion an Molekülen, die eine Mesomerie enthalten, kann es passieren, dass der Substituent an der Mesomerie teilnehmen kann. Dadurch wird das mesomere System vergrößert. In diesem Fall hat der Erstsubstituent einen mesomeren Effekt (kurz: M-Effekt). Mesomere Effekte beeinflussen jede weitere Reaktion an dem betreffenden Molekül. Sie bestimmen, an welcher Position – also an welchem Atom – eine weitere Reaktion wahrscheinlich ablaufen wird. Außerdem ergeben sich mehr mesomere Grenzformeln, wodurch das Molekül stabilisiert wird.
Der Effekt wirkt auf Reaktionsgeschwindigkeiten und Ionengleichgewichte, weil die p- oder π-Orbitale eines Substituenten mit dem Rest des Moleküls überlappen. Es kommt zur Delokalisierung oder deren Erweiterung. Der Effekt wird mit einem M abgekürzt.[1] Daneben gibt es den induktiven Effekt (+I- und –I-Effekt).
Bei der elektrophilen Zweitsubstitution am Benzolring dirigieren (=bestimmen) die Erstsubstituenten die Position der weiteren. Im Allgemeinen kann man sagen, dass Erstsubstituenten, die einen +M-Effekt haben in ortho/para-Stellung dirigieren, solche mit −M-Effekt in meta-Stellung. Dies kann durch die Stabilität der während der Substitution auftretenden Übergangszustände erklärt werden.
+M-Effekt

Der Substituent hat ein freies Elektronenpaar, das er für die Mesomerie zur Verfügung stellen kann. Bei +M-Effekten erhöht sich die Elektronendichte des mesomeren Systems. Eine eventuelle elektrophile Zweitsubstitution wird dadurch begünstigt, der +M-Effekt wirkt somit aktivierend in Bezug auf Reaktivität. Bei Halogenen als Erstsubstituenten ist die Substitutionsgeschwindigkeit allerdings aufgrund des −I-Effektes insgesamt herabgesetzt, dennoch wird durch den +M-Effekt weiter in ortho/para-Stellung dirigiert.
Beispiel: Reaktion von Brom und Benzol: Benzol enthält ein mesomeres System und Brom hat drei freie Elektronenpaare. Nach der Substitution ist Brom mit einer Einfachbindung an ein Kohlenstoffatom des Benzols gebunden. Ein freies Elektronenpaar des Broms kann in die Mesomerie einbezogen werden, wodurch sich neue mesomere Grenzstrukturen ergeben.
Substituenten mit +M-Effekt
−M-Effekt
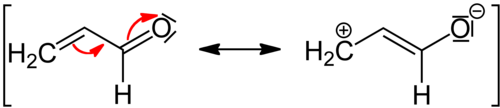
Bei −M-Effekten wird dem mesomeren System Elektronendichte entzogen, da der Substituent eine Doppel- oder Dreifachbindung besitzt. Das erschwert weitere Substitutionen bzw. setzt die Aktivierungsenergie, die dazu nötig ist, herauf. Der −M-Effekt wirkt also aus reaktionskinetischer Sicht deaktivierend. Außerdem wirken die folgenden Gruppen meta-dirigierend.
Substituenten mit −M-Effekt
Säurestärke
Substituenten mit −M-Effekt bewirken eine Erhöhung der Säurestärke von aromatischen, aciden Verbindungen, da sie das entstehende Anion der Säure stabilisieren. Nitrophenole sind im Vergleich zu Phenol (pKs = 9,99) stärkere Säuren. Trinitrophenol erreicht einen pKs-Wert von 0,29.
Basenstärke
Bei einem aromatischen Ring, an dem sich eine Aminogruppe befindet, werden aufgrund des +M-Effektes Elektronen in den Ring gedrückt. So wird die funktionelle Gruppe positiver, der pKb-Wert steigt insgesamt für diese Verbindung. Das heißt, die „Basenstärke“ nimmt ab.
Einzelnachweise
- ↑ Eintrag: mesomeric effect. In: IUPAC Compendium of Chemical Terminology (the “Gold Book”). doi:10.1351/goldbook.M03844 (Version: 2.1.5).