Kupfercitrat
| Strukturformel | ||||||||
|---|---|---|---|---|---|---|---|---|
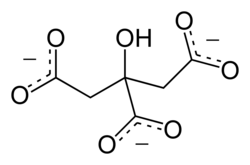
| ||||||||
| Allgemeines | ||||||||
| Name | Kupfercitrat | |||||||
| Andere Namen |
| |||||||
| Summenformel | C12H10Cu3O14 | |||||||
| CAS-Nummer |
| |||||||
| Kurzbeschreibung |
hellblauer Feststoff[1] | |||||||
| Eigenschaften | ||||||||
| Molare Masse | 568,84 g·mol−1 (wasserfrei) | |||||||
| Aggregatzustand |
fest | |||||||
| Löslichkeit |
schwer löslich in Wasser [2] | |||||||
| Sicherheitshinweise | ||||||||
| ||||||||
| LD50 | ||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||
Kupfer(II)-citrat ist das Kupfersalz der Citronensäure.
Beschreibung
Kupfercitrat ist ein kristalliner Feststoff, mit einer für Kupferverbindungen charakteristischen blauen Farbe. Es ist in Wasser nahezu unlöslich.[2]
Herstellung
Kupfercitrat lässt sich beispielsweise durch Reaktion von Kupfer(II)-hydroxid (Cu(OH)2) mit Citronensäure herstellen:
Alternativ kann man Kupfercitrat auch durch die elektrochemische Umsetzung von mit Wasser verdünnter Citronensäure und Kupfer gewinnen.
Verwendung
Kupfercitrat wird in der Önologie zur Behandlung des Weinfehlers „Böckser“ – ein Geruchs- und Aromafehler – verwendet. Kupfercitrat wird dabei als granuliertes „Kupzit“ (mit 5 % Gehalt an Kupfercitrat) dem Wein zugegeben. Dies führt allerdings dazu, dass dann freie, geschmacklich völlig unzulängliche, Kupferionen im Wein verbleiben. Diese müssen daher nach der Böckser-Behandlung mit Kaliumhexacyanidoferrat(II) abgefangen werden, welches die freien Kupferionen weitgehend in eine unlösliche und somit vom Wein abfiltrierbare Form überführt.[4]
Daneben wird Kupfercitrat noch als Algizid in Schwimmbädern, als Antiseptikum, in Metallbearbeitungsölen[1] sowie schon seit 1849 als Pigment[5] verwendet. In geringem Umfang wird das Citrat zur Holzkonservierung eingesetzt. [6] Auch in Nahrungsergänzungsmitteln ist es für das Spurenelement Kupfer als Komponente enthalten.
Sicherheitshinweise
Kupfercitrat ist als gesundheitsschädlich eingestuft und verursacht Augenreizungen.[2] Bei Hamstern zeigte Cu(II)-citrat nach einer Gabe an trächtige Tiere eine fruchtschädigende Wirkung, vorwiegend Missbildungen des cardiovaskulären Systems.[7][8] Die akute Letale Dosis bei Ratten beträgt bei oraler Aufnahme 1.580 mg/kg.[3]
Einzelnachweise
- ↑ 1,0 1,1 Kupferchemikalien. S. 11.
- ↑ 2,0 2,1 2,2 2,3 Sicherheitsdatenblatt (Erbslöh), eingesehen am 29. Dezember 2008
- ↑ 3,0 3,1 Kupfercitrat bei ChemIDplus
- ↑ Weinbehandlung mit Kupfercitrat.
- ↑ N. Eastaugh, V. Walsh, T. Chaplin, R. Siddall: Pigment Compendium: A Dictionary of Historical Pigments. Butterworth-Heinemann, 2004, ISBN 978-0-7506-5749-5
- ↑ T. G. Townsend, H. M. Solo-Gabriele: Environmental Impacts of Treated Wood. CRC Press, 2006, ISBN 978-0-8493-6495-2
- ↑ M. J. Derelanko, M. A. Hollinger: Handbook of Toxicology. CRC Press, 2002, ISBN 978-0-8493-0370-8
- ↑ NRC (USA): Mineral Tolerance of Domestic Animals. National Academy of Sciences, Washington, 1980
Literatur
- A. J. Davison, R. T. Hamilton: Stimulation of cytochrome c oxidation by a copper citrate complex., in: Arch. Biochem. Biophys. 126, 1968, S. 228–231; PMID 5671065.
- Abdelaziz Madinzia, Mohammed El Amanea, Hamid Atmani: Synthesis, characterisation and electrochemical properties of the copper citrate complexes., in: Annales de Chimie Science des Materiaux 25, 2000, S. 179–185; doi:10.1016/S0151-9107(00)88893-5.
- F. J. Di Carlo: Syndromes of cardiovascular malformations induced by copper citrate in hamsters. In: Teratology 21, 1980, S. 89-101. PMID 7385058