Glykogenolyse
| Übergeordnet | ||
| Glykogen-Metabolismus Abbau der Glucane | ||
| Gene Ontology | ||
|---|---|---|
| QuickGO | ||
Unter der Glykogenolyse (Synonym: Glykogenabbau) versteht man den physiologischen Abbau von Glykogen zu Glucose-1-phosphat und Glucose.
Der umgekehrte Prozess ist die Glykogensynthese.
Physiologie
Die Glykogenolyse dient dem temporären Ausgleich fehlender Nahrungsglukose. Die Muskeln nutzen das in ihnen gespeicherte Glykogen selbst, die Leber kann durch die Glykogenolyse auch anderen Organen Glucose zur Verfügung stellen.
Auslöser für die Glykogenolyse ist ein vermehrter Energiebedarf des Körpers, und die damit verbundene Ausschüttung von Glukagon und Adrenalin. Insulin hemmt hingegen die Glykogenolyse.
Biochemie
Glukagon führt in der Leberzelle zu einer Aktivierung von cAMP und zu einer gesteigerten Produktion des Enzyms Glykogenphosphorylase (vgl. Abbildung). Die Glykogenphosphorylase baut den linearen Anteil des Glykogens ab, in dem die Glucose-Moleküle alpha-1,4-glykosidisch miteinander verbunden sind. Dort katalysiert das Enzym die Bindung freien Phosphats am C1-Atom der Glucose. Die glykosidische Bindung zwischen den Glucose-Molekülen wird dadurch aufgespalten. Als Produkt entsteht Glucose-1-phosphat, welches dann noch zur intrazellulären und verwertbaren Form, dem Glucose-6-phosphat, umgebaut (isomerisiert) wird.
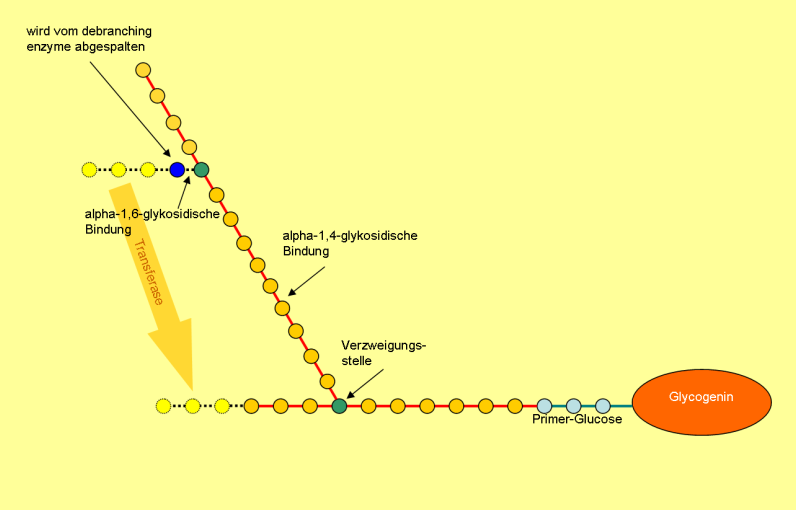
Die Glykogenphosphorylase kann das Glykogen allerdings nur bis zum vierten Glucose-Molekül vor der nächsten Verzweigungsstelle abbauen. Um den weiteren Abbau zu ermöglichen, entfernt die Transferasedomäne des so genannten debranching enzyme drei der vier Glukose-Moleküle vor der Verzweigungsstelle und fügt sie an einer anderen Seitenkette linear (also alpha-1,4-glykosydisch gebunden) an. Die Glucose-Moleküle dieser Seitenkette können nun wieder einzeln durch die Glykogenphosphorylase abgespalten werden.
Das verbleibende Glucose-Molekül, das alpha-1,6-glykosidisch gebunden ist, wird vom Glucosidaseteil des debranching enzyme abgespalten. Dabei entsteht kein Glucose-1-Phosphat, sondern freie Glucose. So führt die Verzweigung des Glykogens dazu, dass bei der Glykogenolyse zu etwa 90 % Glucose-1-Phosphat entsteht, und nur etwa 10 % freie Glucose.
| Bitte den Hinweis zu Gesundheitsthemen beachten! |
| Dieser Text basiert ganz oder teilweise auf dem Flexikon, einem Wiki der Firma DocCheck und ist unter GNU-FDL lizenziert. |